- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Применение спектрофотометрии в фармацевтическом анализе
Для подтверждения подлинности лекарственных средств спектрофотометрическим методом используют несколько подходов. Самый распространенный – это сравнение спектров анализируемого образца и стандартного образца этого же вещества.
В этом случае используют стандартные образцы (Reference Materials, Reference Standards, Reference Substances) вещества, достаточно однородные и стабильные в отношении некоторых специфических свойств, которые признаны подходящими к применению при проведении измерений или испытаний указанных свойств.
Согласно определению, приводимому в Руководстве по надлежащей лабораторной практике (Good Laboratory Practice, GLP) стандартным образцом называется любой объект, принятый в качестве образца сравнения, который сам не является исследуемым объектом. Так, в анализе готовых лекарственных форм используются рабочие стандартные образцы (образцы серийной субстанции, отвечающие требованиям соответствующего стандарта качества лекарственных средств).
Для анализа фармакопейных субстанций применяются государственные стандартные образцы (стандартные образцы, параметры качества которых регламентируются фармакопейной статьей, утвержденной в установленном порядке). Раствор стандартного образца должен быть приготовлен в тех же условиях и с применением тех же растворителей, что и раствор испытуемого вещества.
Спектры веществ должны совпадать по положению максимумов, минимумов и плато, а величины светопоглощения в максимумах не должны различаться более чем на 3%. В этом случае результат анализа наиболее достоверен, однако существенно осложняет работу дефицит и высокая стоимость стандартных образцов.
При отсутствии стандартного образца допускается указание в нормативной документации максимумов и минимумов светопоглощения, которые следует сравнивать с данными, полученными при анализе. Так, в фармакопейной статье, регламентирующей качество экстракта солодки, имеется указание «УФ-спектр раствора, приготовленного для количественного определения, в области от 200 до 360 нм должен иметь максимум при длине волны (258 ± 2) нм».
Иногда при испытании на подлинность рассчитывают удельный показатель поглощения в максимуме и сравнивают его со значением, приведенном в нормативной документации. Это позволяет решить вопрос с дефицитом стандартных образцов, но, в то же самое время, такие методики имеют существенный недостаток: на результат анализа влияют характеристики прибора.
Для решения этой проблемы используют довольно удобный прием: для вещества рассчитывают отношение величин абсорбции при двух максимумах. Такой способ рекомендуют, например, при анализе цианокобаламина – «отношение оптических плотностей А361/А550 должно составлять от 3,10 до 3,45; отношение оптических плотностей А361/А278 должно составлять от 1,70 до 1,9».
Иногда при проведении испытания аналитик сталкивается с необходимостью повышения чувствительности и/или специфичности методики определения. В этом случае целесообразно использовать метод дифференциальной спектрофотометрии, когда к анализируемому веществу добавляют специфический реактив. Дифференциальная спектрофотомерия применяется в анализе многих лекарственных веществ.
Довольно часто этот метод используется для анализа флавоноидов – к извлечению, содержащему исследуемый флавоноид, добавляют 3% спиртовый раствор хлористого алюминия. Раствор выдерживают 40 минут и, в случае необходимости, доводят до нужной концентрации. Параллельно, в тех же условиях, готовят раствор рабочего стандартного образца флавоноида и «нулевой» раствор – из того же извлечения, но без добавления стандартного образца. Это позволяет получить спектры поглощения без наложения абсорбции сопутствующих веществ.
Похожие приемы используют для анализа аминокислот – так, при спектрофотометрическом определении таурина к раствору добавляют нингидрин, доводят рН и температуру до «точки оптимума», выдерживают раствор в течение некоторого времени и снимают спектр полученного окрашенного комплекса.
Одним из вариантов дифференциальной спектрофотометрии является так называемая ΔЕ – спектрофотометрия, когда фиксируют изменение оптической плотности, произошедшее в результате перехода вещества из одной таутомерной формы в другую. Так, при анализе производных барбитуровой кислоты, используют метод, предложенный В.Г. Беликовым: спектр поглощения раствора снимают при разных значениях рН. При значении рН = 2 барбитурат существует в виде лактамной формы, при изменении рН до 10 – переходит в лактимную, а при дальнейшем увеличении водородного показателя (рН =13) – в дилактимную (рисунок 1).
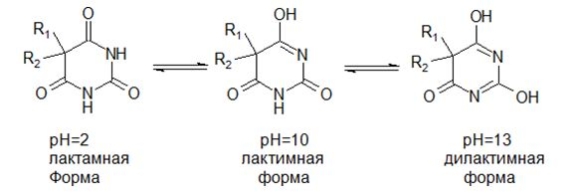
Рисунок 1. Лактим-лактамная таутомерия барбитуратов
Спектр поглощения при этом также претерпевает изменения, что позволяет не только идентифицировать производные барбитуровой кислоты, но и дифференцировать их по положению заместителей.
Так, 5,5 – замещенные барбитуратов в лактамной (имидной) форме не имеет хромофорной системы (сопряженных простых и двойных связей), абсорбирующей электромагнитное излучение в УФ – области. Молекула в лактимной (имидольной) форме такую систему уже имеет, способна к абсорбции в данной области и имеет максимум светопоглощения при 240 нм.
Дилактимная (диимидольная) форма имеет еще одну двойную связь – хромофорная система удлиняется, и в спектре происходит батохромный сдвиг. Максимум светопоглощения при этом смещается в область 255-260 нм (рисунок 2).
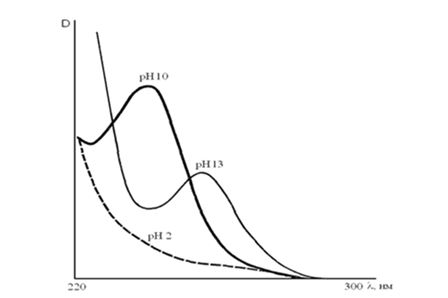
Рисунок 2. Изменение спектра поглощения 5,5-замещенных барбитуратов в зависимости от рН раствора
Барбитураты, имеющие в молекуле три заместителя, способны к существованию только в одной ионизированной таутомерной форме – лактамной и имеют максимум светопоглощения при 245 нм, который не смещается при изменении рН.
Спектр поглощения тиобарбитуратов имеет по два максимума при рН = 2 (239 и 260 нм) и при рН = 10 (255 и 310 нм), в сильнощелочной среде, при рН=13, наблюдается один максимум (310 нм).
Таким образом, применение спектрофотометрии может дать некоторые представления о свойствах исследуемых веществ (наличие и изменение хромофорных и ауксохромных групп). Так, наличие в структуре лекарственного вещества фенольного гидроксила имеются полосы поглощения при 251, 257 и 263 нм, замещенные ароматические радикалы обуславливают максимум светопоглощения при 260 нм, сопряженные двойные связи – при 238 нм.
(Макиева М.С., Морозов Ю.А., Морозова Е.В., Морозов В.А. Оптические методы анализа лекарственных средств, ИПЦ Сев. Осет. гос. ун-т им. К. Л. Хетагурова)
Статьи по теме
- Рамановская спектроскопия
- Применение БИК-спектроскопии в фармацевтическом анализе
- Строение и принцип работы БИК-спектрометра
- Применение ИК-спектроскопии в фармацевтическом анализе
- Порядок работы на ИК-спектрометре
- Строение и принцип работы ИК-спектрометра
- Инфракрасная спектроскопия
- Порядок работы на фотоэлектроколориметре
- Фотоэлектроколориметрия
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

